查驗中心以促進產業發展、增加國際競爭優勢及建立諮詢服務之品質、透明化及一致性為目的,於 2018年1月1日起推出「付費諮詢服務」方案,明訂諮詢服務項目包含三大項目:
- 臨床試驗申請案預審(IND Prior Assessment):依申請者須要,分為品質部分、非臨床部分或完整技術性資料之事先評估。此類諮詢服務因藥品複雜程度分為化學藥及生物製劑。
- 臨床試驗諮詢(Clinical Trial Consultation):包含第一期至第四期臨床試驗設計相關諮詢。
- 研發策略諮詢(Regulatory consultation services):包含銜接性試驗策略評估、查驗登記策略評估及其他計畫書諮詢等項目。
申請者可在藥品開發期間、申請臨床試驗前及申請銜接性試驗評估/查驗登記前等各種時程,依據需求提出諮詢服務申請。諮詢流程包含:申請者線上填寫申請表、策略商談、查驗中心受理後成立諮詢團隊提供深入之法規科學建議、以書面意見及諮詢會議形式回覆申請者。申請者須於正式送件時一併檢附該書面意見及會議紀錄,作為查驗中心日後審查之重要參考依據。
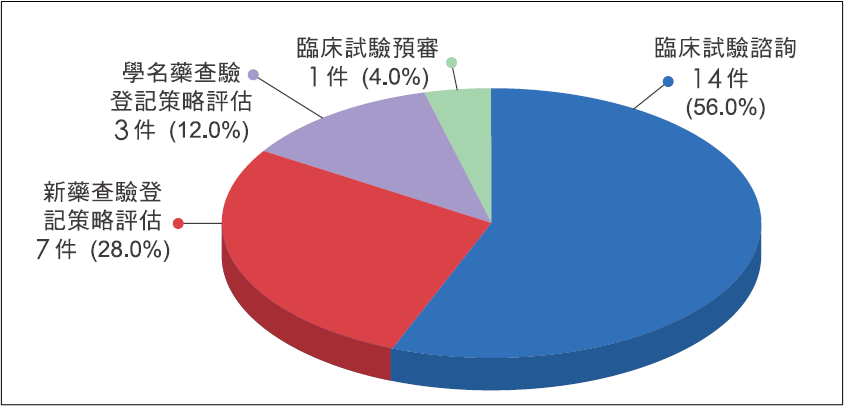
2024年藥品付費諮詢案件結案計有25件。以案件類別區分,臨床試驗諮詢14件,新藥查驗登記策略評估7件,學名藥查驗登記策略評估3件,臨床試驗預審1件。案件數及所占百分比如下圖。
歷年成果詳如年報所示:連結至年報頁面
查驗中心自 2005 年起建立指標案件諮詢輔導服務機制,組成專屬諮詢輔導團隊,提供國內生技製藥與學研機構,在醫藥品研發各階段之法規科學建議,期望藉由主動式的深入諮詢輔導,降低醫藥品研發成本,縮短研發時程。
指標案件輔導對象涵蓋國產廠商/生技業者、學術與研究機構,早期是由查驗中心向國內產學研單位以定期主動徵求、公開甄選方式進行。自2012 年起,則改成隨到隨評的方式,將申請案依創新程度、貢獻程度、早收程度、滿足法規程度等四面向進行評估及篩選。評選後獲同意列入指標案者,由查驗中心與申請方正式簽約,並由輔導團隊與申請方共同確立年度預定目標、訂定案件之各階段性目標,召開諮詢輔導會議,主動掌握專案研發進度。查驗中心針對指標案件之諮詢輔導建置有主動積極輔導機制,提供不同研發期程之國內外專業法規參考資訊,與全方位的法規諮詢服務,期能協助國內醫藥產業發展並促成成功案例。
2024年間持續輔導的藥品指標案件總計77件,其中有11件為2024年新增指標案。2024 年提供法規科學諮詢的次數總計有38件次。
依案件的研發期程、藥品分類及申請者分別分析如下: 以藥品研發期程分類,於臨床前階段有32件,在一期臨床試驗階段11件,在二期臨床試驗階段13件,在三期臨床試驗階段14件,申請查驗登記階段1件,獲得查驗登記核准函6件。
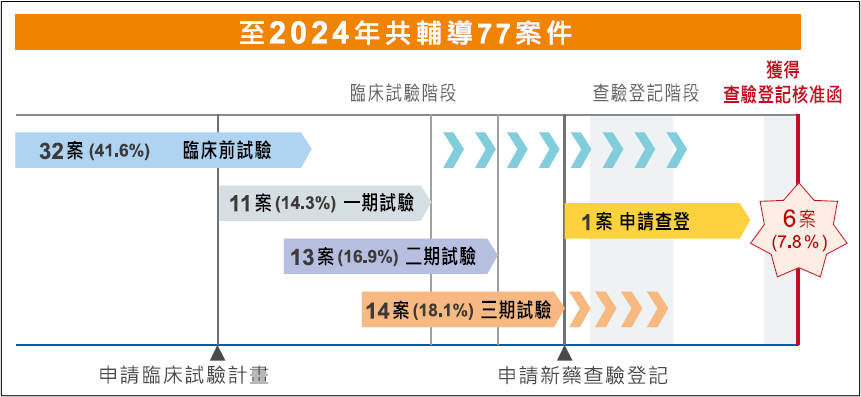
為呈現藥品指標案件之輔導成果,依藥品開發歷程設定以下五個輔導成果里程碑:通過臨床試驗申請案進入一期臨床試驗、通過臨床試驗申請案進入二期臨床試驗案、通過臨床試驗申請案進入三期臨床試驗、申請新藥查驗登記、獲得查驗登記核准函、及上市後研究核准。
2024年度成功達成上述里程碑者計有5件:獲得一期臨床試驗核准1件,獲得二期臨床試驗核准1件,獲得三期臨床試驗核准1件,申請新藥查驗登記1件,及獲得上市後研究核准1件。
歷年成果詳如年報所示:連結至年報頁面
申請者可依據產品研發期程、案件屬性和法規需求提出諮詢。查驗中心就申請者提出的諮詢議題和相關技術性資料,進行專案研究,以書面 / 諮詢會議等方式,提供不同研發階段之法規需求及試驗設計相關建議,以作為研發策略規劃之參考。
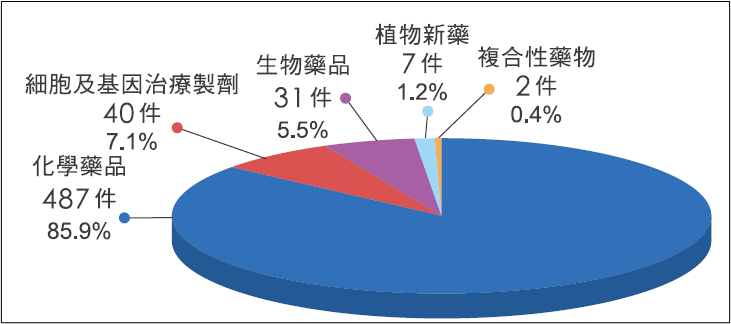
2024 年查驗中心完成藥品法規諮詢案共計567件。以藥品類別區分,依諮詢藥品類別分析,計有化學藥品487件,細胞及基因治療製劑40件,生物藥品31件,植物新藥7件,複合性藥物2件。
歷年成果詳如年報所示:連結至年報頁面
查驗中心於 2024 年執行藥品與醫療器材研發法規諮詢與輔導評估業務,共進行藥品類案件 16 件,其中包括計畫審查5件及計畫進度評估11件。經濟部科專計畫之法規科學評估相關書面建議及查證,藥品共109件。
歷年成果詳如年報所示:連結至年報頁面