藥品上市後業務
藥品風險管理計畫及執行成效報告評估
- 更新日期:2024-12-29
- 點閱次數:4997
「風險管理計畫」係以用藥安全為出發點之管理策略,依藥品之風險程度執行各項降低風險的措施,例如:病患用藥說明書、醫療人員通知、特殊風險預防措施等不同程度之風險管理措施,並定期檢視風險管理計畫執行成效,以有效降低國人用藥風險。為協助藥商提出符合要求之風險管理計畫並落實其執行,我國於101年4月5日公告「藥品風險管理計畫及內容格式參考指引」。
依據藥品查驗登記審查準則第三十八條之一,申請新成分新藥查驗登記無檢附出產國許可製售證明與採用證明(non-CPP)者或屬國內自行研發之新成分新藥,須提供上市後風險管理計畫;其他新藥或已上市藥品,如經藥品安全性評估,認定應執行風險管理計畫必要者,亦應依產品風險等級之不同,進行相關之上市後風險管理。以下內容將介紹藥品風險管理計畫之送件,最新公告請至台灣藥物法規資訊網查詢。
- 審查案件類型:
- 風險管理計畫與計畫變更:
- 依藥品查驗登記審查準則第三十八條之一規定,申請查驗登記之新成分新藥 (含生物藥品),無檢附出產國許可製售證明與採用證明 (non-CPP)。
- 屬國內自行研發之新成分新藥。
- 其他經衛生福利部食品藥物管理署認定,須檢送風險管理計畫者。
- 風險管理計畫執行成效評估報告。
- 風險管理計畫與計畫變更:
- 申請應檢附資料:
- 風險管理計畫:請檢送公文 (敘明申請事由)、風險管理計畫書。
- 風險管理計畫變更:請檢送公文 (敘明申請事由)、原核准計畫書 (註明版本日期)、修正後計畫書、計畫書修正前後對照表(敘明修正原因)。
- 風險管理計畫執行成效評估報告:請檢送公文 (敘明申請事由)、核准計畫書 (註明版次/版本日期)和成效評估報告。
- 注意事項:
- 藥品風險管理計畫經審查通過後,如認為計畫有變更之必要者,應向衛生福利部食品藥物管理署提出計畫變更申請。
- 請依衛生福利部同意之風險管理計畫 (版次/版本日期:)確實執行,並根據風險管理計畫所訂時程,定期提供執行成效報告。請確實依風險管理計畫之「執行方法」執行,如發放medication guide、定期舉辦教育訓練、特殊風險預防措施等,並評估其執行成效;請詳實收集AE、SAE案例,並對AE與藥品的相關性進行評估,以及評估是否有新增之藥品安全性警訊。
- 風險管理計畫格式及內容說明,請參考藥品風險管理計畫書 (範例)以及藥品風險管理計畫追蹤報告格式 (範例)。
- 風險管理計畫之撰寫以中文為原則。
- 收件窗口:
| 案件狀態 | 受文者 | 紙本收件地址 |
|---|---|---|
| 新申請案/申復案 | 衛生福利部食品藥物管理署 | 國家生技園區F棟 (地址:11571台北市南港區研究院路一段130巷99號) |
| 補件/申請補件延期 | 正本: 財團法人醫藥品查驗中心 |
財團法人醫藥品查驗中心 (地址:11557台北市南港區忠孝東路六段465號3樓) |
| 副本: 衛生福利部食品藥物管理署 |
國家生技園區F棟 (地址:11571台北市南港區研究院路一段130巷99號) |
- 風險管理計畫審查流程:
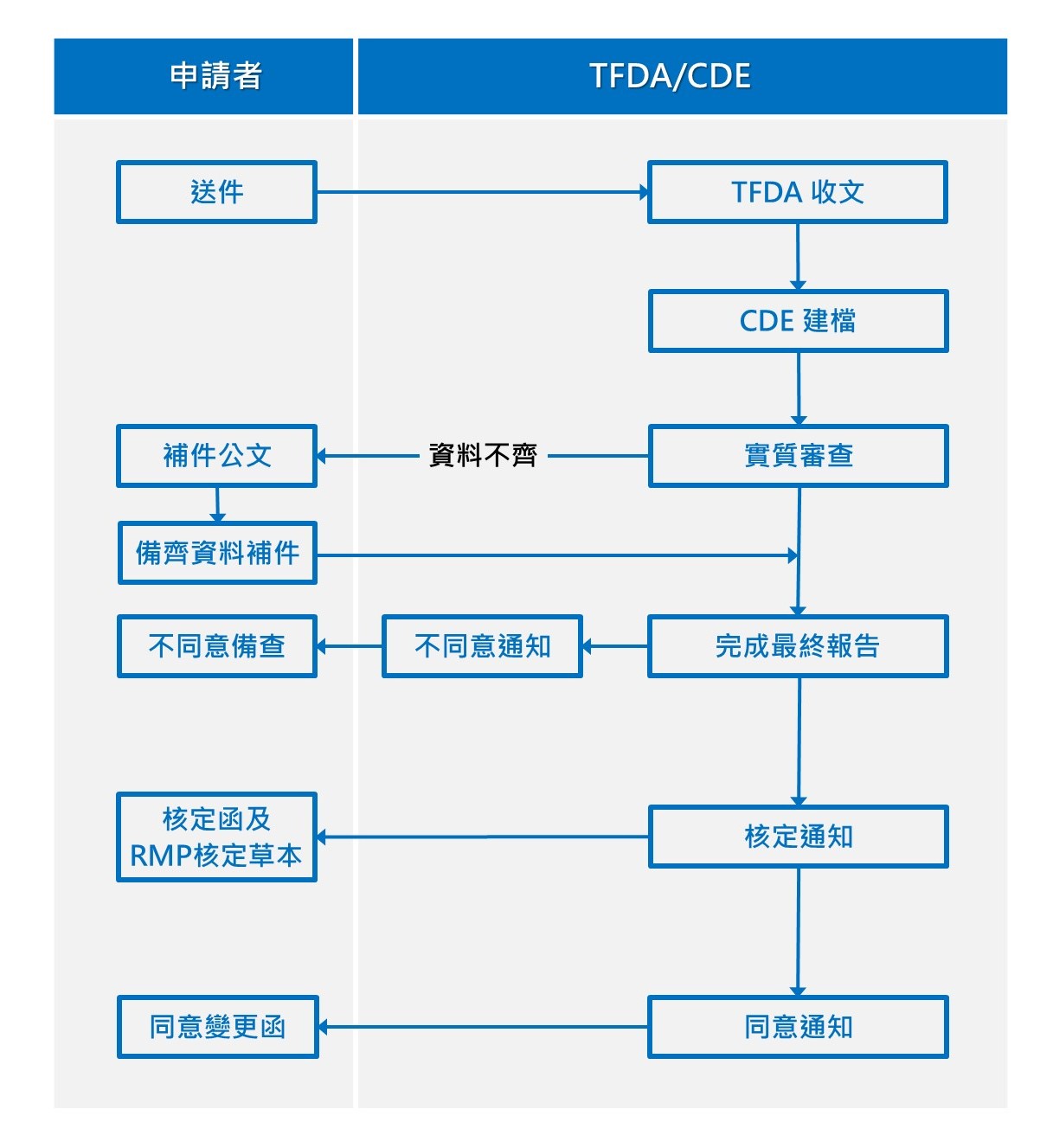 相關注意事項:
相關注意事項:
(一)申請人如未能於期限內補正者,得於補正期滿前,以書面敘明理由申請延期;其延期期限,自補正期滿翌日起算一個月,且延期以一次為限。
(二)基於風險管理原則,技術性資料審查後,如有特殊議題須諮詢專家委員意見,將視需要諮詢外部委員或提送藥品諮議小組討論。
(三)若對函文內容有疑問,可連絡案件承辦人或申請審查案件函文釋疑。
(四)有關案件審查進度,可至衛生福利部食品藥物管理署網站>藥品>案件申辦進度查詢。
- 諮詢服務
本中心具豐富的國內外法規科學知識及多年審查經驗,提供業者及研發單位在藥品於研發至上市各階段多元法規諮詢服務,歡迎各界先進多加利用,以利準備符合法規要求之送審文件,如欲提出申請,請詳見諮詢服務。
無須收取規費。
檔案下載
| 序號 | 名稱 | 檔案類型 | 檔案大小 |
|---|---|---|---|
| 1 | 藥品風險管理計畫書(範例) |
|
58.9KB |
| 2 | 藥品風險管理計畫追蹤報告格式(範例) |
|
101.4KB |
